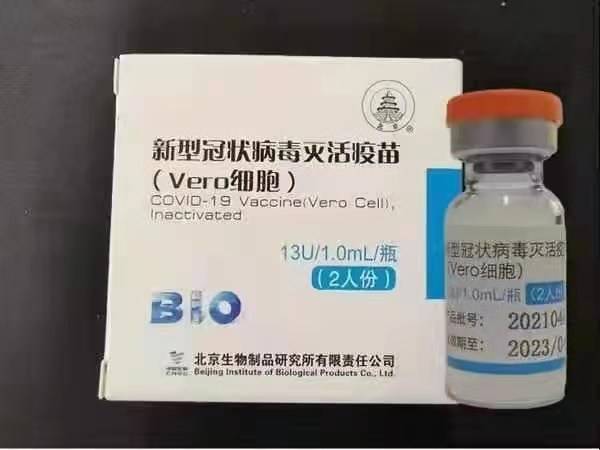
Sinopharm (Pekin): BBIBP-CorV
FAZ 1
1 Deneme
ChiCTR2000032459
Çin
FAZ 2
2 Deneme
NCT04962906
Arjantin
ChiCTR2000032459
Çin
AŞAMA 3
6 Deneme
NCT04984408
ChiCTR2000034780
Birleşik Arap Emirlikleri
NCT04612972
Peru
NCT04510207
Bahreyn, Mısır, Ürdün, Birleşik Arap Emirlikleri
NCT04560881, BIBP2020003AR
Arjantin
NCT04917523
Birleşik Arap Emirlikleri
Onaylar
DSÖ Acil Kullanım Listesi 59 Ülke
Angola, Arjantin, Bahreyn, Bangladeş, Beyaz Rusya, Belize, Bolivya (Çokuluslu Devlet), Brezilya, Brunei Sultanlığı, Kamboçya, Kamerun, Çad, Çin, Komorlar, Mısır, Ekvator Ginesi, Gabon, Gambiya, Gürcistan, Guyana, Macaristan ve Guyana 、 İran (İslam Cumhuriyeti) 、 Irak 、 Ürdün 、 Kırgızistan 、 Lao Demokratik Halk Cumhuriyeti
Lübnan 、 Malezya 、 Maldivler 、 Moritanya 、 Auritius 、 Moğolistan 、 Karadağ 、 Fas 、 Mozambik 、 Namibya 、 Nepal 、 Nijer 、 Kuzey Makedonya 、 Pakistan 、 Paraguay 、 Peru 、 Filipinler 、 Kongo Cumhuriyeti 、 Enegal 、 Sırbistan 、 Seyşeller 、 Sierra Leone 、 Adalar、Somali、Sri Lanka、Tayland、Trinidad ve Tobago、Tunus、Birleşik Arap Emirlikleri、Venezuela (Bolivarya Cumhuriyeti)、Viet Nam、Zimbabve
Sinopharm BBIBP-CorV COVID-19, patojenik yeteneği olmayan kültürde yetiştirilen virüs parçacıklarından yapılan inaktive bir aşıdır. Bu aşı adayı, Sinopharm Holdings ve Pekin Biyolojik Ürünler Enstitüsü tarafından geliştirildi.
Sinopharm BBIBP-CorV aşısı, bağışıklık sisteminin SARS-CoV-2 beta koronavirüse karşı antikor üretmesini sağlayarak çalışır. Kuduz aşısı ve hepatit A aşısı gibi inaktive virüs aşıları on yıllardır kullanılmaktadır. Bu geliştirme teknolojisi, kuduz aşısı gibi birçok iyi bilinen aşıya başarıyla uygulanmıştır.
Sinopharm'ın SARS-CoV-2 suşu (WIV04 suşu ve kütüphane numarası MN996528), Çin'in Wuhan kentindeki Jinyintan Hastanesindeki bir hastadan izole edildi. Virüs, yetkin bir Vero hücre hattında kültür içinde çoğaltıldı ve enfekte olmuş hücrelerin süpernatanı, 48 saat boyunca β-propiolakton (1:4000 hacim/hacim, 2 ila 8°C) ile inaktive edildi. Hücre kalıntılarının netleştirilmesinden ve ultrafiltrasyondan sonra, ilk inaktivasyon ile aynı koşullar altında ikinci bir β-propiolakton inaktivasyonu gerçekleştirildi. WHO'ya göre, aşı 0,5 mg şap üzerine emdirildi ve koruyucu içermeyen 0,5 mL steril fosfat tamponlu salin içinde önceden doldurulmuş şırıngalara yüklendi.
31 Aralık 2020'de Devlet İlaç İdaresi, Sinopharm tarafından geliştirilen deneysel aşının onaylandığını duyurdu.
7 Mayıs 2021'de Dünya Sağlık Örgütü aşının onaylandığını duyurdu. DSÖ'nün acil kullanım listesi, ülkelerin COVID-19 aşısını ithal etmek ve uygulamak için kendi düzenleyici onaylarını hızlandırmalarını sağladı. DSÖ Bağışıklama Stratejileri Danışma Uzman Grubu da aşı incelemesini tamamladı. Mevcut tüm kanıtlara dayanarak, WHO, 18 yaş ve üstü yetişkinler için üç ila dört hafta arayla iki doz aşı önermektedir. Semptomatik ve hastanede yatan hastalığa karşı aşı etkinliğinin tüm yaş grupları için toplamda %79 olduğu tahmin edilmektedir.
Amerikan Tabipler Birliği, 26 Mayıs 2021'de "A Randomize Clinical Trial: Effect of 2 Inaktive SARS-CoV-2 Aşısının Yetişkinlerde Semptomatik COVID-19 Enfeksiyonu Üzerindeki Etkisi" yayınlayarak, "rastgele bir klinik araştırmanın bu önceden belirlenmiş ara analizinde, Yetişkinler Randomize klinik çalışmaların bu önceden belirlenmiş ara analizinde uygulanan 2 etkisizleştirilmiş SARS-CoV-2 aşısı, semptomatik COVID-19 riskini önemli ölçüde azalttı ve ciddi yan etkiler nadirdi." Erişkinlerde yapılan bu faz 3 randomize çalışmada, semptomatik COVID-19 vakalarında 2 inaktive edilmiş tam virüs aşısının etkinliği sırasıyla %72.8 ve %78.1 idi. 2 aşıda, sadece şap içeren kontrol grubuna benzer sıklıkta nadir görülen ciddi advers olaylar vardı ve çoğu aşı ile ilgisizdi. Bir keşif analizi, 2 aşının, faz 1/2 deneyinin sonuçlarına benzer şekilde, ölçülebilir nötralize edici antikorları indüklediğini buldu.
DSÖ SAGE Çalışma Grubu, 10 Mayıs 2021'de Sinopharm/BBIBP COVID-19 aşısının bir incelemesini yayınladı. GAVI'nin COVID-19 aşısı, sağlık çalışanlarına aşının uygun şekilde saklanıp saklanmadığını ve aşıya maruz bırakılıp bırakılmadığını söyleyen bir aşı şişesi monitörü içerir. aşırı ısınma Sonuç olarak, GAVI, 14 Mayıs 2021'de hasar bildirdi. Zebra Technologies tarafından üretilen ve Temptime Corporation tarafından yapılan akıllı etiketler, ortasında daha açık renkli bir kare bulunan bir daireden oluşur ve zaman içinde geri dönüşü olmayan bir şekilde renk geliştiren renksiz bir kimyasaldan yapılmıştır. . Bu, kümülatif ısıya maruz kalmanın görsel bir göstergesini vermek için daha koyu hale gelir. Şişe optimal saklama aralığının ötesinde ısıya maruz kaldığında, kare daireden daha koyu hale gelir ve bu da aşının artık kullanılmaması gerektiğini gösterir.
Ulusal İlaç BBIBP-CorV COVID-19 aşı ilaç kütüphanesi kayıt numarası: DB15807.